

フィリオ30と複合洗浄消毒システムについて
複合洗浄消毒システムにおける洗浄消毒には、フィリオ30という高濃度500ppmの次亜塩素酸弱酸性水溶液を使用します。
次亜塩素酸においては、多くの商品が出回っております。しかし、下記の国が定める次亜塩素酸のガイドラインである食安基発第0825001号に含まれておらず、HCVなどに有効(製品独自の第三者検査機関によるHCV不活性化試験結果による)濃度500ppmなのは特許生成法の次亜塩素酸弱酸性水溶液のフィリオ30だけです。
他の次亜塩素酸製品を食安基発第0825001号における1の二液生成法・2の電解生成法に振り分けていきたいうと思います。念のため申しますが、振り分けられた製品は店内・家庭での除菌や消臭に使用するぶんには問題ありません。複合洗浄消毒システムには使用しないでください。
食安基発第0825001号
各
都道府県
保健所設置区
特別区
衛生主管部(局)長 殿
厚生労働省医薬食品局
食品安全部基準審査課長
次亜塩素酸ナトリウムに酸を混和して使用することについて
標記について、食品添加物「次亜塩素酸ナトリウム」を食品添加物である「塩酸」又は「クエン酸」 等の酸と混和して使用する事例等について都道府県等から照会があり、解釈について疑義を生じている 向きがあるので、下記の点に留意の上、貴管内関係者に対する周知徹底方よろしくお願いする。
記
なお、食品添加物「次亜塩素酸ナトリウム」と食品添加物である「塩酸」又は「クエン酸」等をあら かじめ混和した水溶液を販売することは、この当該水溶液中で化学反応が生じていると考えられること から、添加物製剤には該当せず、その販売は認められない。
2. また、平成11年6月25日衛化第31号厚生省生活衛生局食品化学課長通知「いわゆる電解水 の取扱いについて」の2において、食品添加物「次亜塩素酸ナトリウム」を希釈したものと同等と取り 扱われているいわゆる電解水についても、上記1と同様に取り扱うものとする。
「上記1の補足」
食品添加物「次亜塩素酸ナトリウム」と食品添加物である「塩酸」又は「クエン酸」等をそれぞ れ組み合わせて販売〜というのは、それぞれの薬剤を混ぜない状態で、次亜塩素酸用のセット販売するのは良いという意味です。
「複合消毒システム」は法定消毒薬でもある塩素系消毒薬に属するフィリオ30(原液500ppm)を用いた「洗浄消毒」というプロセスと共に、法定消毒を尊守することで互いに効果を発揮いたします。システムは洗浄消毒として「第一次洗浄消毒」、そして法定消毒を消毒作用/目的毎に別けて「第二次基礎消毒」「第三次保管消毒」と、より公衆衛生としての現場を意識した複合的なプロセスで成り立っているのです。
・洗浄消毒というプロセス
まず洗浄消毒というプロセスの意味としては、第二次基礎消毒の効果を高めることにあります。消毒対象物に付着した血液、汗などや、細菌/ウィルスなどの有機体を洗浄し、第二次基礎消毒へ繋げる事が目的。その結果、基礎消毒で使用するエタノールなどの作用効果を高め、その溶液内の汚染を最小限にするものとします。この場合の「洗浄」とは、有機体の蛋白質をフィリオ30の作用により分解してしまうことを意味し、流水によるものだけではありません。補足になるが、医療現場でも使用されるグルタラール消毒薬は、厚生労働省により「対象物を60分以上流水にて洗浄してから浸漬する事」とされています。これを怠ると、薬液作用により細菌/ウィルスの外層蛋白質を硬化させてしまい、その後の消毒作用に大きく影響を与えるのです。結果的に浸漬容器の消毒液内は汚染され、消毒液内における二次感染を引き起こす可能性があります。そのような事からも、理美容店においても洗浄消毒は大変重要な意味を持つと考えます。
・複合洗浄消毒システムの特徴
フィリオ30の原液500ppmを「危機管理濃度」として使用し、対象物の血液負荷状態を想定しています。血液を想定するという事は、蛋白質汚染であり、その先には汗なども含まれると考えます。また、対象物の使用状態/目的により100ppm(五倍希釈)を「衛生管理濃度」、50ppm(十倍希釈)を「衛生環境濃度」として、水で希釈して使用すます。「衛生管理濃度」「衛生環境濃度」は、対象物へ直接噴霧して使用するが、危機管理濃度として500ppmの原液を使用する際に、システムの特徴として「ティッシュペーパー」を使用する事にあります。実際の作業とすると、使用済み剃刀を流水で洗浄をします。その後、剃刀をティッシュペーパーで挟むように包み込み、フィリオ30を満遍なく十分に噴霧。放置後に、ティッシュペーパーで余分な水分を拭き取り後に廃棄して、剃刀は第二次基礎消毒「エタノール溶液浸漬」へ移行いたします。多枚刃などの剃刀でも、挟んだティッシュペーパーに満遍なく十分に噴霧する事により、対象物に次亜塩素酸が密着して浸漬効果となります。放置後の剃刀などについた水分をティッシュペーパーで拭くことができ、作業工程も容易になる訳です。従来は水分を拭く作業には清潔な布などが指定されていたが、ティッシュペーパーであれば使用毎の使い捨てになります。ウェットティッシュよりもコストは安く、使用するフィリオ30も平均5cc程で済む為にコスト的にも優れています。容易な事とコストは営業形態問わず重要な事であり、継続性に繋がるシステムといえます。

理美容店での消毒(血液汚染器具を想定)作業に使用する際の注意点
様々な弱酸性の次亜塩素酸製品が販売されておりますが、理美容室で消毒剤として現場使用する際の最低条件です。

- ナトリウムが生成過程で除去され、ほとんど含まれていない。
- 酸(塩酸・酢酸)を使用していない。
- 血液汚染器具に対応できる500ppmの濃度。
- 濃度が製品に明記されている。
- 生成年月が製品に明記されている。
- 製品における第三機関データがある。
- 消毒対照にノロウィルスではなく肝炎ウイルスを想定している。

・純度の高い次亜塩素酸である事。
生成過程で、「次亜塩素酸ナトリウム」と「水」以外が含まれない事が大事。また殺菌作用がある「次亜塩素酸」以外の不純物が含まれないということ。また、原材料として使用している次亜塩素酸ナトリウムは「特級」(最高ランク)のものを使用しております。
・ナトリウムが殆ど含まれていない。
製造過程でナトリウムが取り除かれ、殆ど含まれていないということは、副産物としてのNaCl(塩)発生による鋏や剃刀の刃など(スチールは除く)金属腐食などの影響が少ないということ。ただし「低濃度だから金属腐食しない弱酸性次亜塩素酸」と混同しないこと。
・漂白・変色・変型の心配が殆どいらない。
爆発的な反応で、直ぐに水と塩素に分解される為に、漂白・変色・変型などの心配はいりません。ただし、色物タオルは「タオル生地」「染め方法」により色落ちする場合がありますので、目立たない箇所に噴霧して5分ほど放置して確認してください。特に「青」「茶」系統の色合いのものには、気をつけてください。
・トリハロメタンの心配もない。
水道水などに含まれる環境汚染物質(臭素など)が水道法に基づく0.01mg/L以下の基準値であること~またその検査結果が明記できていること。水道水と同等の安全性がある、ということ。
・塩酸などが生成段階で含まれない。
「二液式」製法ではないということ。次亜塩素酸ナトリウムを水で希釈する代わりに「塩酸」で希釈する「弱酸性次亜塩素酸」を生成する一番多い手法。生成時には塩素ガスが発生し、高濃度になるほど発生量が多い。ネットなどで^弱酸性次亜塩素酸水」として調べると、殆どの製品がこの生成法にあたる。塩酸が含まれる「弱酸性次亜塩素酸」は理美容室での洗浄消毒使用は向かないと思われる。製品説明では明記されていないので注意が必要。
・生成後の経時変化が大きい「電解式」は理容店での消毒には不向き。
「電解式」で製法される「弱酸性次亜塩素酸水」は「塩」と「水」で電解器から生成されて使用するには問題はないが「低濃度」なので理美容室での洗浄消毒使用は向かないと思われる。「二液式」と組み合わせボトリングされた製品も存在するが、生成されてからの品質変化が大きいとされ、同じく理美容室での洗浄消毒使用は向かないと思われる。
・「緩衝式」で生成しているのが最適。
この国際特許製法の生成方法であると製品に明記されていること。現在、高濃度製品(500ppm)のものは「フィリオ30」のみ。
・製造年月が明記されている生成水。
医薬品ではないので表示義務はないが、生成された年月が刻印されていること。理美容室での洗浄消毒作業用としては最低条件として考える。
・製品に500ppm以上の濃度表記がキチンとされている。
製品の効果説明に使用している濃度と、製品として販売されている濃度が違う場合があるために製品を見分ける基準。理美容室における洗浄消毒作業においての「原液」とは500ppmとして考えます。
・香がまったくない商品は、有効濃度に注意。
無臭とする製品は、有効成分の濃度に注意すること~低濃度になれば「無臭」になるために注意が必要。極端な刺激臭がするのも理美容室での使用は注意が必要である。
・血液付着を想定した検査結果をもっている。
理美容室での洗浄消毒作業においては、菌やウィルス単体で消毒する環境よりも「タンパク質(血液)」もふくまれた環境下での作業が主となる。ゆえに、そのような状況下での試験データに基づいた殺菌効果をもつ消毒液が理想とします。
・消毒作用後(反応後)の安全性。
殺菌やウィルスと反応した後は、フィリオ30自体は水と塩素に分解されます。噴射した器具は数分自然乾燥した後に流水で流して、エタノールや逆性石鹸液へ浸けてください。洗浄の際にフィリオ30の残留成分で、配管を痛めたりすることはありません。
・噴霧処理を主な方法とする。
殺菌後のフィリオ30自体は水と塩素に分解されてしますので、そのあとは殺菌作用はありません。ゆえに、「漬け置き消毒」での消毒液の「使い回し」的な使用方法には不向きです。「漬け置き消毒」の際には原液を使用せず、5倍希釈(100ppm)で使い捨てと考えてください。理美容店では対象物に噴霧して、自然乾燥(1分以上)してから流水で洗浄するのが第一次洗浄消毒と考えます。

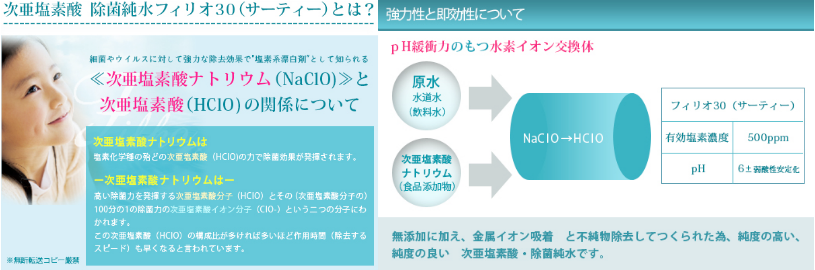
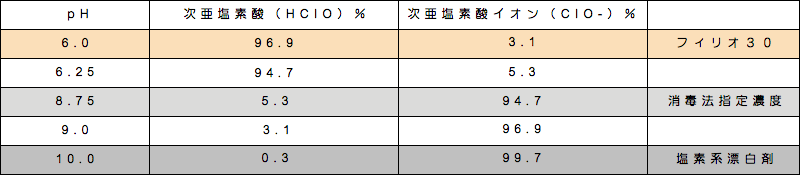
「次亜塩素酸HCIO」と「次亜塩素酸イオンCIO-」の割合比
「塩素系消毒剤」としての消毒力は次亜塩素酸ナトリウム中の細胞壁表面への酸化成分である「次亜塩素酸イオン CIO-」と、細菌/ウィルス内部まで浸透して強い酸化作用を起こす「次亜塩素酸 HCIO」の割合比によって大きく変ります。理美容室で使用している「塩素系漂白剤」はおおよそPH10、また消毒法で定められている希釈100ppmですと、pH8.75。「次亜塩素酸イオン CIO-」が90%以上を占めており、細菌/ウィルス内部まで浸透して強い酸化作用を起こす「次亜塩素酸 HCIO」は1割以下の状態。フィリオ30はpH6で「次亜塩素酸(殺菌成分」96.9%になります。さらに他の製法にはできない純度の高い「次亜塩素酸(殺菌成分)」ですので、その消毒力は従来の塩素系消毒剤の約80倍。理美容室では、第一次洗浄消毒剤として、最高の働きをしてくれます。
弱酸性ということ。
「次亜塩素酸 HCIO(殺菌成分)」が多いpH6 まで水で薄めて近づける、という事。
アルカリ性の家庭用漂白剤(次亜塩素酸ナトリウム)を弱酸性にするために「水」で薄める、という方法があります。理美容師の消毒法でも「水」で100ppm まで希釈するとありますが、希釈することにより酸性に近づけて殺菌力をあげている事実があります。では、実際に「水」で薄めてpH を調整するとどうなるのか?12%次亜塩素酸ナトリウム(病院用ハイターなどは6%)を水で薄めていくと、pH7付近になると、濃度が「1ppm以下」になってしまい、理美容室の現場では殆ど使う用途がありません。 そこで「水」の代わりに「塩酸」を使用したのが「二液式」で生成された次亜塩素酸になりますが、基本的には厚生労働局では販売を認めておりません。
フィリオ30は「緩衝法」生成された安全・安定したpH6の弱酸性です。
フィリオ30の強い消毒力と酸化力は、高濃度で存在する次亜塩素酸 HClOにあります。pH6域において多く存在する次亜塩素酸 HClOは電荷を帯びておらず、分子型であるために細菌における細胞膜やウイルスにおけるエンベロープなど、脂質二重膜を通り抜けることができるのです。ゆえに細菌やウイルス内部において、活動をする上で重要な蛋白質を酸化させて性質変化および、機能を停止させることができる訳です。細菌においては、代謝機能を司る酵素(蛋白質)などの重要な働きをする蛋白質を酸化し変化させる為に、死にいたります。ウイルスは、寄生する細胞内で自身を複製する際に重要な働きをするヌクレオカプシドを構成する蛋白質を酸化させ性質変化および分解してしまうので、核酸を複製する事ができず、不活性化状態になるのです。ちなみに、アルカリ性域で多く存在する次亜塩素酸イオン ClO-などは、脂質二重膜を通り抜けられないために、表面の蛋白質を酸化させて変化させるに止まるので、消毒対象体によっては十分な効果が得られません。次亜塩素酸イオンは、鉄表面に酸化鉄(錆)を付着させますが、次亜塩素酸の場合は鉄などに対する酸化作用は強く反応し溶出させるがゆえに、表面に酸化鉄(錆)を付着させず溶液内でも飽和状態になるために大きく進行はしません。ただし剃刀の刃(替刃)に関しては、鉄の溶出と共に刃先研ぎ面に影響が出る為に、長時間の浸漬には向きません。
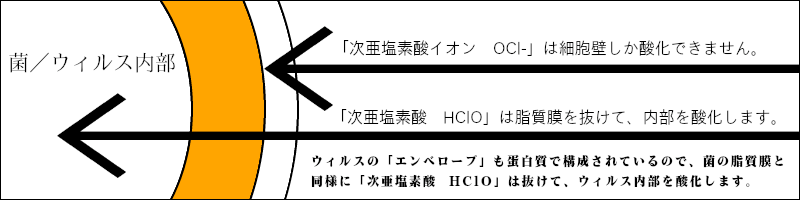
内部から破壊する「次亜塩素酸 HClO」
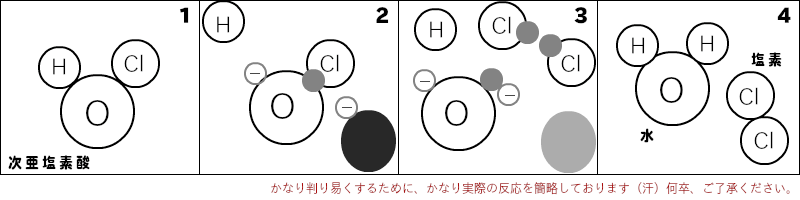
殺菌システムは力な爆発的なラジカル反応~酸化作用にあり
1
次亜塩素酸(HClO)の安定した状態です。
2
有機物(蛋白質)を見つけちゃうと、酸素(O)は水素(H)から電子を奪ってポイッと離しちゃいます。残った陰電子を帯びた(イオン化した)酸素(O・)と塩素(Cl・)は「ラジカル」という険悪な不安定な関係になります。ちなみにこの状態は「ClO・」となり、一酸化塩素ラジカルという不安定~ラジカル反応状態になります。次亜塩素酸(HClO)と共にpH状態で存在する「OCl-」も同じ構成ですが、こちらは「次亜塩素酸イオン」といい、有機物(蛋白質)などから電子を奪う酸化作用は起きるものの、安定した関係(不安定ながらも未練がある関係?)なので酸化反応速度(攻撃力)が違います。
3
ラジカルな関係になった塩素ラジカル(Cl・)は自分が安定した幸せな状態になるためにサッサと逃げ出し、逃げられるやいなや酸素ラジカル(O・)は有機物(蛋白質)から電子を奪ってしまいます・・電子を奪われた有機物(蛋白質)は性質が変って本来の働きを機能しなくなったり、分解したりしちゃいます。これって「ラジカル」な関係が壊れた末の事件なワケです・・ちなみに、酸素(O)の電子を奪い取る行動・・これが「酸化」といい、奪い取られた有機物(蛋白質)の性質を変化させてしまい、溶菌(不活性化)となるわけです。
4
ハッと、気が付くと独りになっちゃった酸素(O)は、慌てて水素(H)を呼び戻すワケです・・しかも2つも。で、水(H2O)という安定した状態になりまして一件落着。一方、自分の幸せ「ラジカルな関係」を求めた塩素(Cl)は同じ価値観を持つ塩素(Cl)を見つけて、安定した塩素(Cl2)になりまして、これまた一件落着・・と、いうワケです。
フィリオ30は、この酸素(O)の行動が桁外れに盛ん・・もとい、活発なワケです。つまり、「菌」を見つけると、もの凄い勢いで何もかも捨てて飛びついちゃうワケです。しかも、主成分である次亜塩素酸(HClO )は菌でいえば「細胞壁」までしか攻撃(酸化)できない次亜塩素酸イオン(OCl-)とは違い、下層の「脂質膜」をも通り抜け細胞内部に到達して、強力な酸化作用を行います。これが、脅威の溶菌(不活性化)力になります。生成法の関係からPH6.5(+-0.5)弱酸性の安定した状態で、「無添加」で不純物(塩酸などの混ざり物)がない「高濃度」である・・つまり、菌に対して爆発的な反応をする環境が整っている、というのがフィリオ30というワケです。
・「蒸し器」「紫外線消毒器」「煮沸消毒器」「エタノール」「逆性石鹸」「ヒビテン」「次亜塩素酸ナトリウム(家庭用塩素系漂白剤)」などの消毒法による作業前の第一次洗浄消毒剤に最適。
・原液での使用の場合は、「フィリオ30自体が反応後に水と塩素に分解してしまう」「強力な酸化作用」がある為に、エタノールや逆性石鹸のような「浸け置き消毒」には向いておりません。スプレーによる噴霧使用がフィリオ30の特色と殺菌力を活かす使用方法かと思います。
・理美容室での「血液付着が認められない」場合は、塩素系消毒薬の消毒法指定でもある5倍希釈の100ppm濃度で十分です。この場合は「浸け置き」消毒も可能ですが、使用したフィリオ30を使い回ししないでください。
現行の消毒法におけるシステムを、より完璧にする為の第一次洗浄消毒剤として使用します。タンパク質/菌/ウィルスを速やかに除去した上で、保健所指定の各法令下の消毒システムとの複合消毒システムを行うことにより、効果を最大限に活かすことができます。理美容室での使用方法としては、対象器具へ噴射後に数分自然乾燥をしてください。その後に流水で流してから、複合消毒として消毒法下の作業を行ってください。
重要なお知らせ
一部の業者に「次亜塩素酸」というキーワードで相談し、「家庭用漂白剤(次亜塩素酸ナトリウム)でも薄くして使用すれば大丈夫」といわれ、数十倍に希釈して超音波噴霧器などに使用する事例がでております。目などに傷みや、部屋内の金属/加湿器内などが腐食するなどの弊害がでてます。「次亜塩素酸」というキーワードだけで、取り入れると非常に危険です。
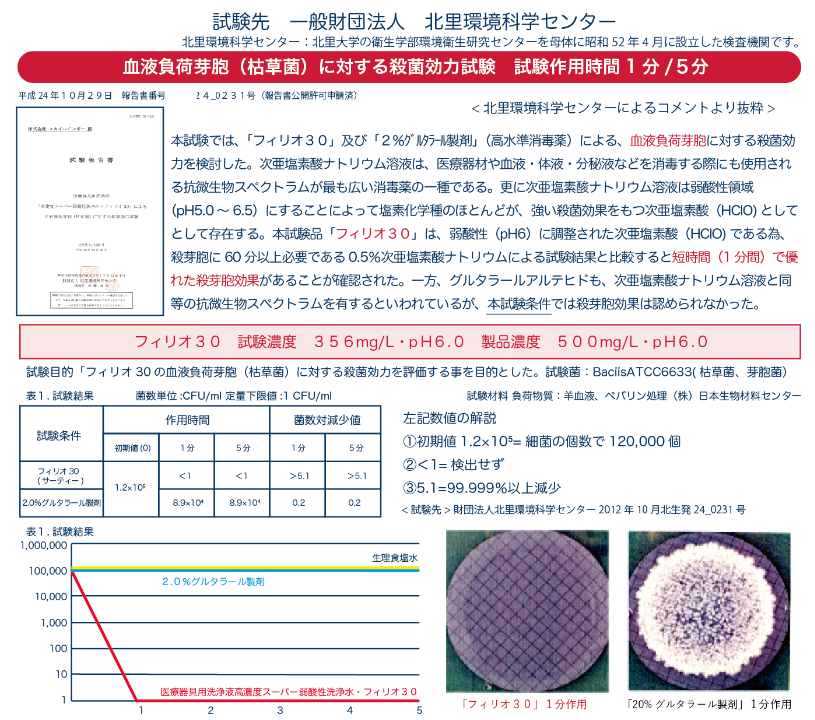


フィリオ30の濃度別使用法
原液500ppm「危機管理濃度」血液汚染が予想される器具への使用。

5倍希釈100ppm「衛生管理濃度」器具を洗浄消毒することにより、二次感染を未然に防ぎます。

10倍希釈「衛生環境濃度」20倍希釈「衛生生活濃度」細菌や、臭いなどの環境を整えます


第三者である試験機関による製品独自の試験結果が存在するということが大切です。理容師は国家資格者です。ですので、キチンとした製品独自データがあることが我々のえ「衛生管理」にとっては最低条件になります。公開されている「成分の効果」を流用したり、実際に販売されている製品の濃度よりも濃い濃度での試験結果を表示したりする薬剤は使用するべきではありません。
下記のエビデンスは複合洗浄消毒システムにおける指定衛生管理品の製造販売元から提出された製品独自データになります。学術的データを引用・転用する製品はシステムには使用できません。更に複合洗浄消毒システムの確実性のために製造販売元に理容室まで出向いていただき、実際の施術工程でのATP検査などで実証データを作成しております。ですので、システムを独自に解釈して方法を変更したり、別薬剤などを使用したものには「一切適応されません」ので御了承ください。
エビデンス
一般には、医学および保健医療の分野では、ある治療法がある病気・怪我・症状に対して、効果があることを示す証拠や検証結果・臨床結果を指す。エビデンスは、医療行為において治療法を選択する際「確率的な情報」として、少しでも多くの患者にとって安全で効果のある治療方法を選ぶ際に指針として利用される。

【血液汚染器具に対する除タンパク効果】
実験的に血液で汚染させた歯科用器具を、医療器具用洗浄液「高濃度次亜塩素酸弱酸性水溶液・フィリオ 30」浸漬後に、器具に残留するタンパク質を定量して、除タンパク効果を確認することを目的とした。
【試験水】
- 医療器具用洗浄液「高濃度次亜塩素酸弱酸性水溶液・フィリオ 30」;原液使用 (有効塩素濃度 500 mg/L、pH 6.0 ± 0.5)(実測値:有効塩素濃度 356mg/L、pH6.0)
【試験材料】
- 汚染対象品:歯科用器具「ミラートップ」(「Dental Mirror」吉田ミラートップ#4)
- 汚染物質:羊全血, ヘパリン処理 ((株)日本生物材料センター)
【試験条件】
- 1) ミラートップへの血液塗布 ミラートップに血液0.01mLを塗布した (写真1参照)。洗浄方法
- あらかじめ25 ± 2°Cに保持した試験水50 mLを100 mL容量のガラス容器に分取し、血液塗布したミラートップを所定時間浸漬した。所定時間浸漬後に1%SDS (Sodium n-Dodecyl Sulfate) 10 mLが入った試験管内にミラートップを回収し、10分間超音波洗 浄機 (BRANSON 2210J, 90W) で処理後さらにボルテックスミキサーで撹拌して、 ミラートップに残留している血液を洗い出したものを、タンパク質定量用試料液とした。水道水浸漬条件は、試験水浸漬後に、水道水50 mL中に浸漬し、その後は前記同様の方 法で洗い出した。血液塗布直後に、浸漬せずに洗い出したものを、「初発」とした。
- タンパク質の定量 タンパク質定量用試料液を室温で1時間静置後、 BCA法で試料液1 mLあたりのタンパク質量を定量した (定量下限値 1.0 g/mL)。
- 有効塩素濃度およびpH測定 試験直前に試験水「フィリオ30」の塩素濃度をAQUABAQ-102(柴田科学, ヨウ素法) で、pH を CMPACT pH METER, B-212 (HORIBA, ガラス電極法) で測定した。 また、すすぎ水として用いた「水道水」の残留塩素濃度を Pocket Colorimeter (HACH, DPD法) で測定した。
【試験結果】
「フィリオ 30」に 5 分間浸漬後のミラートップに残留したタンパク質量は、17 g/mL (除去率 89.4%) 、水道水に 30 秒間浸漬後は 6.2 g/mL (除去率 96.1%) となった。一方、「グルタラール製剤 2.0%」に 5 分間浸漬後のミラートップに残留したタンパク 質量は、初発とほぼ同等の数値である 170 g/mL となり、水道水に 30 秒間浸漬したも のは 100 g/mL (除去率 37.5%) となった。「フィリオ 30」と「グルタラール製剤 2.0%」での浸漬洗浄による残留タンパク質量 の除去率を比較すると、5 分間浸漬後で「フィリオ 30」は「グルタラール製剤 2.0%」 の 10 倍、水道水 30 秒間すすぎ後では 10 倍以上の除去率差が認められた。
【牛下痢症ウイルス(C型肝炎ウイルス代替)の不活性化試験】
「次亜塩素酸弱酸性水溶液フィリオ30」のウシ下痢症ウイルス(C型肝炎ウイルス代替)に対する不活化効果を評価した。
【試験水】
- 医療器具用洗浄液「高濃度次亜塩素酸弱酸性水溶液・フィリオ 30」;原液使用 (有効塩素濃度 500 mg/L、pH 6.0 ± 0.5)(実測値:有効塩素濃度 414mg/L、pH6.0)
【試験材料】
- 供試ウイルスの培養と調製方法:BVDVをウシ腎臓由来細胞株に感染させ、細胞培養面積の約90%以上が細胞変性効果を示したときー80度の冷蔵庫に凍結保存した。その後、凍結融解操作を2回繰り返し、3,500rpmで10分間遠心した上澄みを摂取し、限外ろ過膜で濃縮したウイルス液を供試ウイルスとした。
【試験結果】
初期ウイルス感染価は5.8x10の4乗PFU/mLリットルであった。PBS(陰性対象)に30秒間作用させた場合の感染価は3.5x10の4乗PFU/mLであり、初期値からほとんど変動しなかった。一方「高濃度次亜塩素酸弱酸性水溶液フィリオ30」をウイルスに30秒間作用させた場合、検出限界値(5PFU/mL)以下となった。
【血液負荷芽胞(枯草菌)に対する殺菌効力試験】
医療器具用洗浄液「高濃度弱酸性次亜塩素酸水フィリオ30」の血液負荷芽胞(枯草菌)に対する殺菌能力を評価することを目的とした。
【試験水】
- 医療器具用洗浄液「高濃度スーパー弱酸性洗浄水・フィリオ 30」;原液使用 (有効塩素濃度 500 mg/L、pH 6.0 ± 0.5)(実測値:有効塩素濃度 350mg/L、pH6.0)
- グルタラール製剤;2.0%に希釈して使用・洗浄前ATP値2,601/洗浄消毒後ATP値44(タンパク除去率98.3%)
【試験材料】
負荷物質:羊血、ヘパリン処理(株式会社日本生物材料センター)
試験菌:枯草菌、芽胞液(NAMSA社製lot.GBS009-08)
【試験結果】
初期値は1.2x10の5乗CFU/mLであった。対照の生理食塩液に5分間作用させた場合の菌数は1.2x10の5乗CFU/mLであり、初期値から変動しなかった。試験品「フィリオ30」を血液負荷芽胞に1分間作用させた場合、定量下限値(1CFU/mL)未満となり、菌数対数減少値を示した。一方、試験品「2%グルタラール製剤」の5分間作用後の菌数は9.8x10の4乗CFU/mLとなり、対象と比較してほぼ変わらなかった。以上より「フィリオ30」は、作用時間1分でLRV=5.1以上の値を示しており、血液負荷芽胞に対する殺菌効果があると判断された。一方「2%グルタラール製剤」は作用時間5分での殺菌効果は認められなかった。
【芽胞(枯草菌)に対する殺菌効力試験】
【試験水】
- 医療器具用洗浄液「高濃度次亜塩素酸弱酸性水溶液・フィリオ 30」;原液使用 (有効塩素濃度 500 ppm、pH 6.0 ± 0.5)
- 塩素系漂白剤/次亜塩素酸ナトリウム;原液5%使用(50,000ppm)
【試験材料】
試験菌:枯草菌6.6x10の9乗(66,000,000個)
【試験結果】
・塩素系漂白剤:放置時間30秒間/生菌数<1(検出されず)
・フィリオ30:放置時間30秒間/生菌数 1個
【浸漬試験】
【試験水】
- 医療器具用洗浄液「高濃度次亜塩素酸弱酸性水溶液・フィリオ 30」;5倍希釈液使用 (有効塩素濃度 100 ppm、pH 6.0 ± 0.5)
【試験材料】
合成ゴム、ステンレス(歯科用シリコンポイント)ポリカーボネート樹脂(歯科用開口器)、プラスチック、ゴム(歯科用バキュームホース及びホルダー)、鏡器具(歯科用ミラートップ)、スチール(歯科用スチールバー)
【浸漬時間】
2時間
【試験結果】
- 合成ゴム
- ステンレス(歯科用シリコンポイント)/変化は観察されなかった。
- ポリカーボネート樹脂(歯科用開口器)/変化は観察されなかった。
- プラスチック/変化は観察されなかった。
- ゴム(歯科用バキュームホース及びホルダー)/変化は観察されなかった。
- 鏡器具(歯科用ミラートップ)/変化は観察されなかった。
- スチール(歯科用スチールバー)/腐食が観察された。
【浸漬試験】
【試験水】
- 医療器具用洗浄液「高濃度次亜塩素酸弱酸性水溶液・フィリオ 30」;5倍希釈液使用 (有効塩素濃度 100 ppm、pH 6.0 ± 0.5)
【試験材料】
スチール(歯科用スチールバー)
【浸漬時間】
10分間
【試験結果】
- スチール(歯科用スチールバー)/腐食は観測されなかった。
【フィリオ30の解放オープンパッチテスト】
【試験品】
- 医療器具用次亜塩素酸弱酸性水溶液「フィリオ30」 (有効塩素濃度 200 ppm、pH 6.0 ± 0.5)
【判定基準】
「皮膚刺激性・感作性試験の実施法と皮膚性状計測および評価」 皮膚刺激性試験 ヒトパッチテストに準じた皮膚 判定基準にて実施。
【評価方法】
医師が判定基準に従って評価(塗布60分後、塗布24時間後)
【試験結果】
- オープンパッチテストにおける皮膚刺激指数は、フィリオ30の200ppmについては、0.0 であり、安全品であった。
【食品衛生及び平成15年厚生労働省告示第261号26項目検査】
【試験品】
医療器具用洗浄液「高濃度次亜塩素酸弱酸性水溶液・フィリオ 30」5倍希釈液使用 (有効塩素濃度 100 ppm、pH 6.0 ± 0.5)
【検査結果】 検査対象:水質基準/検査結果:数値
- 一般細菌:100CFU/mL以下/検査結果:0
- 大腸菌:不検出/検査結果:不検出
- カドミウム:0.01mg/L以下/検査結果:0.001mg/L未満
- 水銀:0.0005mg/L以下/検査結果:0.00005mg/L未満
- 鉛:0.1mg/L以下/検査結果:0.001mg/L未満
- ヒ素:0.05mg/L以下/検査結果:0.001mg/L未満
- 六価クロム:0.05mg/L以下/検査結果:0.005mg/L未満
- 硝酸態窒素及び亜硝酸態窒素:10mg/L以下/検査結果:1.6mg/L未満
- フッ素及びその他の化合物:0.8mg/L以下/検査結果:0.12mg/L未満
- 有機リン:0.1mg/L以下/検査結果:0.001mg/L未満
- 亜鉛:1.0mg/L以下/検査結果:0.005mg/L未満
- 鉄:0.3mg/L以下/検査結果:0.005mg/L未満
- 銅:1.0mg/L以下/検査結果:0.005mg/L未満
- マンガン:0.3CFU/mL以下/検査結果:0.005未満
- 塩素イオン:200mg/L以下/検査結果:34mg/L
- カルシウム、マグネシウム等:300mg/L以下/検査結果:3mg/L
- 蒸発残留物:500mg/L以下/検査結果:140mg/L未満
- 隠イオン界面活性剤0.5mg/L以下/検査結果:0.002mg/L未満
- フェノール類0.005mg/L以下/検査結果:0.0005mg/L未満
- 有機物等:10mg/L以下/検査結果:0.2mg/L未満
- pH値:5.8~8.6/検査結果:pH6.5
- 味:異常なし/検査結果:異常なし
- 臭気:異常なし/検査結果:異常なし
- 色度:5以下/検査結果:0.4
- 濁度:2以下/0.1未満
- シアン:0.01mg/L以下/検査結果:0.001mg/L未満
【考察】
26検査項目全ての水質基準数値を下回る結果となった。よって、誤飲による障害はないことが立証された。ただし、飲料水ではないので、故意的に口に含んだり飲料はしないこと。

ATP測定法(ATPそくていほう)とは、すべての生物の細胞内に存在するATP(アデノシン三リン酸)を酵素などと組み合わせて発光させ、その発光量(Relative Light Unit;RLU)を測定する方法のことである。ATPふき取り検査とも呼ばれる。細胞内の存在するATPは、酵素であるルシフェラーゼなどと反応させることにより発光する。この発光量はATP量が多いほど発光量(Relative Light Unit;RLU)が増す。この方法を利用して、食品業界や医療機関などでは器具の汚染調査、清浄度調査などに利用されている。これは、細菌や残渣などの汚染物質が残っているとATPが存在し、発光することによりモニタリング法として適切な衛生管理が行うことができるとされている。なお、この検査方法は、厚生労働省監修の「食品衛生検査指針微生物編2004」にも掲載されている。現在、ATP測定法により微生物の同定などを行うことはできない。宇宙開発分野では、惑星などで生物が存在しているかどうかの方法としてATP測定法が活用されている。2001年にキッコーマン株式会社が開発したATP測定器「ルミテスターPD-10」、2009年に発売された「ルミテスターPD-20」は、従来のATPだけではなく、ATPが加熱・変形したAMP(アデノシン一リン酸)も測定することができ、より精密な測定が行えるようになった(特許No.3409962)。
複合洗浄消毒システムATP測定試験
理容店におけるATP検査
【試験日】
平成28年2月11日
【使用薬剤等】
・洗浄ルネサンス(200倍希釈液)
・高濃度次亜塩素酸フィリオ30原液(500ppm)
【計測器具】
・ATP計測器:ルミテスター(キッコーマン製)
【洗浄対象物】
・シェービングブラシ
・替刃式剃刀
【対象物試験方法】
・試験物を理容店にてでた刈毛(人毛)と水溶性性整髪料を混ぜた微温湯に24時間浸漬
【検査方法】
理容店営業中と同じ状況下を想定し、検査を意識しないシンプルな作業を心掛けた。検査体の初期測定値を測る前の流水洗浄においては、法定消毒下で指定されている10秒以上ではなく、付着した刈毛(毛髪)を流す程度にしている。
【検体状態】
・シェービングブラシがこれだけの脂に汚染される環境は、通常の施術環境下では考えられない。しかし、石鹸を使用せずに直接剃った場合や、オイルなど使用した多様化するシェービング技術を踏まえて検査準備をした。
・剃刀はシェービングブラシ同様、通常以上の汚染環境にて浸漬させた。通常の施術環境下では刃部位以外は、シェービング工程において脂などが付着する可能性は低いが、剃刀全体に汚染させている。剃刀本体も新しいと金属部分の汚れが付着しづらいため、あえて10年以上前の古い剃刀を使用した。
【その他】
ティッシュペーパー
【検査結果】
シェービングブラシ/作業時間 1分
1・流水洗浄して計測/5341
2・洗浄ルネサンスをブラシ中心部に噴霧、軽く揉み洗いして水洗して計測/169 除去率96.9%
3・フィリオ30をブラシ中心部に噴霧して計測/96 除去率98.2%
・剃刀/作業時間 1分
・流水洗浄して計測/581
・ティッシュペーパーで包んで洗浄ルネサンス噴霧し、ティッシュにて拭き取り後に計測/207 除去率64.4%
・ティッシュペーパーで包んでフィリオ30を噴霧し、ティッシュペーパーにて拭き取り後に計測/45 除去率93%
【シェービングブラシ測定結果考察】
今回のシェービングブラシは脂に長時間浸漬させているが、実際はシェービングソープ(陰イオン界面活性剤)をブラシ内に含ませているので、最初の流水洗浄で泡と共にかなりの量のタンパク質は除去されると思われる。試験では、あえてタンパク質汚染された状況から行っている。
複合洗浄消毒システムにおける「第一次洗浄消毒」としてブラシ内部に洗浄ルネサンスとフィリオ30を噴霧して計測した。洗浄ルネサンスに含まれる成分(注1)は浸漬することにより効果が発揮されるため、2の計測値は非イオン界面活性剤と流水によるものと考えられる。この工程は「理容師法施行規則第25条」における洗浄工程を「非イオン界面活性剤」でシェービングブラシにも適応しているが、流水工程を増やすことにも意義があると思われる。その後に高濃度次亜塩素酸弱酸性水溶液「フィリオ30」をブラシ中心部に噴霧し、軽く絞った状態で計測しているが、2の数値は変化して最終的には3の数値は98.2%の汚染物質除去率となっている。
フィリオ30原液(500ppm)噴霧後は流水洗浄せずに自然乾燥させるが、その間にフィリオ30の第三者試験機関による効果(注2)が作用していくと考える。フィリオ30は、他生成法(2液/電解生成法)に比べても不純物がなく、次亜塩素酸自体は水に変化する性質とフィリオ30の安全性試験データ(注3)から考えても、その後の施術に使用しても問題ない。因みに、血液汚染の場合は最後にブラシ部分の煮沸消毒工程が必要である。
【剃刀測定結果考察】
クラシカルシェービングては、ラザーリングでの石鹸(陰イオン界面活性剤)において肌上のタンパク質は除去されているため、現場では1の数値程は高くないと推測される。
複合洗浄消毒システムにおける「第一次洗浄消毒」として洗浄ルネサンスのティッシュペーパーでの浸漬拭き取り作業は、「理容師法施行規則第25条」における洗浄工程を「非イオン界面活性剤」で対応している。ただ、行政指導においては「スポンジ」で擦って洗浄とあるが、「スポンジ」の汚染については触れていない。この「スポンジ」は使い捨てと指定されておらず、「使い回し」と考えると「スポンジの衛生管理問題」が発生する。このような理由から、複合洗浄消毒システムではティッシュペーパーを使用している。この時点の2の数値は「207」であり除去率64.4%であるが、これはティッシュペーパーにて物理的にタンパク質が除去されていると思われる。
さらに、再度ティッシュペーパーで剃刀を包んでフィリオ30原液(500ppm)を噴霧する。放置(他の器具の洗浄作業時間程度)した後に、ティッシュペーパーで水分を拭き取り、次の工程「第二次基礎消毒」の「エタノール浸漬」に移行させる。この時点が3の数値で、「45」除去率93%となっている。今回は脂の中に浸漬させて剃刀全体を付着させているための数値であり、通常のシェービング環境下では、更に除去率が高いことが予想される。フィリオ30においては第三者試験機関による効果(注4)が1分以下で不活性化が実証されているので、放置の時間目安としたい。また、ティッシュペーパーによる浸漬により、限られた量による作用になる為に、替刃への影響は考えられない。
エタノールはタンパク質凝固作用もある為に、エタノール浸漬による数値低下は僅かになる。その為、複合洗浄消毒システム下ではエタノール浸漬後の剃刀は第三次保管消毒として、洗浄ルネサンス200倍希釈液に浸漬させて保管させる。成分(注1)の働きでタンパク質98%除去が第三者試験機関により実証(注5)されている。この事から、複合洗浄消毒における「第一次洗浄消毒」「第二次基礎消毒」「第三次保管消毒」工程を経た剃刀はタンパク質汚れが除去され、菌やウイルスの不活性化状態であることが立証される。
注1:酵素・オキシドール成分・炭酸ナトリウム・非イオン界面活性剤(エーテル系)・他
注2:「血液汚染器具に対する除タンパク効果(北生発21_0817_1号)」・「ウシ下痢症ウイルス(C型肝炎ウイルス)不活性化試験(北環発24_0025号)」・「血液負荷芽胞(枯草菌)に対する殺菌効果試験(北生発24_0231号)」
注3:「水質検査結果報告書(報告番号00815934-1)」・「緩衝法次亜塩素酸水溶液の解放オープンパッチテスト」
注4:「ウシ下痢症ウイルス(C型肝炎ウイルス)不活性化試験(北環発24_0025号)」・「血液負荷芽胞(枯草菌)に対する殺菌効果試験(北生発24_0231号)」
注5・医療器具用洗浄剤「洗浄ルネサンス」による血液汚染器具に対する除タンパク効果の検討(北生発25_0350号)
複合洗浄消毒nanoシステムATP測定試験
訪問理容において、訪問先で水道による流水洗浄ができない環境を想定した試験を行った。試験物をフィリオ30ナノにて洗浄消毒を行い、洗浄成分をフィリオ30噴霧により流水洗浄を行っている。
理容店におけるATP検査
【試験実施日】平成27年11月2日
【使用薬剤等】
・分散+殺菌剤:フィリオ30nanoクリーナー(※)
・殺菌剤:フィリオ30(原液および5倍希釈)
【計測器具】
・ATP計測器:ルミテスター(キッコーマン製)
【洗浄対象物】
・剃刀
・シェービングブラシ
・鋏
・トリマー刃
・手指
・布
【その他】
・泡立て用シェービングソープ
・拭取用ティッシュペーパー
・拭取用ウェットティッシュ
【対象物試験方法】
・試験物を理容店にてでた刈毛(人毛)と水溶性性整髪料を混ぜた微温湯に10時間浸漬
【剃刀】
フィリオ30nanoクリーナーを噴霧30秒し、ティッシュペーパーにより拭取ります。その後にフィリオ30原液(500ppm)を噴霧により洗浄成分を洗い流し、エタノールに10分浸漬させ測定。
洗浄前ATP値1,576/洗浄消毒後ATP値0.8(汚染物除去率99.2%)
【シェービングブラシ】
フィリオ30nanoクリーナーを噴霧30秒し、ブラシ部分を揉み込みます。その後にフィリオ30原液(500ppm)を噴霧により洗浄成分を洗い流して測定。
洗浄前ATP値3,424/洗浄消毒後ATP値2.3(汚染物除去率97.7%)
【鋏】
フィリオ30nanoクリーナーを噴霧30秒し、ティッシュペーパーにより拭取ります。その後にフィリオ30原液(500ppm)を噴霧により洗浄成分を洗い流し、ティッシュペーパーで拭取り測定。
洗浄前ATP値2,601/洗浄消毒後ATP値44(汚染物除去率98.3%)
【トリマー(刃部位)】
フィリオ30nanoクリーナーを噴霧30秒し、ティッシュペーパーにより拭取ります。その後にフィリオ30原液(500ppm)を噴霧により洗浄成分を洗い流して測定。
洗浄前ATP値1,406/洗浄消毒後ATP値21(汚染物除去率98.5%)
【考察】
剃刀、シェービングブラシ、鋏、トリマー刃 においては、従来の洗浄方法に較べ、汚れの残留率が格段に下がった。原因は、フィリオ30ナノが油脂やその他の粘性成分を微細化分散させ、粘着した汚れが被洗浄面から遊離し、水流やティッシュにより容易に除去されるようになるためと考えられる。
顕微鏡観察では、シェービングブラシから採取したサンプルを比較すると、洗浄前と較べ、洗浄後のサンプルの方が汚れや細菌のようなものが少なくなっていることが確認できる。
訪問先での複合洗浄消毒システムにおける洗浄過程において、フィリオ30は、殺菌効果を担うものであるのに対して、フィリオ30ナノは洗浄効果を担うものであり、殺菌洗浄工程としては双方を洗浄工程に組み込む必要がある。
細菌はタンパク質汚れの中に存在し、またタンパク質汚れの中で増殖する。また、肝炎やHIVなどのウイルスは血液の汚れの中に存在する。したがって、衛生管理上、殺菌効果を得るためには汚れを除去することが非常に重要であるが、被洗浄面に皮脂の付着があると、水、アルコールなどは油を落とす力が小さいため、皮脂と混ざった汚れが落ちにくい。フィリオ30ナノは皮脂を超微細粒子状に分散させるため、油も汚れも被洗浄面から除去する効果がある。
以上より、水道水による流水洗浄ができない環境下での殺菌洗浄にはフィリオ30ナノを組み込んだ洗浄工程が効果的である。
追加試験
【手指】
試験溶液に浸漬させた手指にフィリオ30nanoクリーナーを噴霧し10秒擦ります。その後にフィリオ30の5倍希釈(100ppm)を噴霧により洗浄成分を洗い流して測定。
洗浄前ATP値2,479/洗浄消毒後ATP値22.8(タンパク除去率99.1%)
【手指】
試験溶液に浸漬させた手指を、アルコールウェットティッシュで拭取り後に測定。
洗浄前ATP値3,406/洗浄消毒後ATP値5,586(タンパク除去率ー64.0%)
【考察】
訪問先で水道水による流水手洗いができないことを想定した試験です。フィリオ30ナノとフィリオ30による洗浄により手指についたタンパク質汚れを除去することができた。しかし、エタノールが含まれたウェットティッシュで拭いた場合では、逆に値が増加しています。これは、ウェットティッシュだけでは感染予防ができないことを示してます。これは手指洗浄する流水施設がない店舗では、技術者の手指が感染源になっている可能性を示唆している。
歯科におけるATP検査・1
【試験実施日】平成27年12月3日
【使用薬剤等】
・分散+殺菌剤:フィリオ30nanoクリーナー(※)
【計測器具】
・ATP計測器:ルミテスター(キッコーマン製)
【洗浄対象物】
・歯科用ミラー
【その他】
・エタノールワッテ
・拭取用ティッシュペーパー
【対象物試験方法】
・従来方法
使用済試験体(洗浄前)をATP計測し、エタノール浸漬20秒から拭取り後にATP計測
・新規方法
使用済試験体(洗浄前)をATP計測し、フィリオ30nanoクリーナー浸漬20秒から拭取り後にATP計測
【従来方法】
洗浄前ATP値27,591/洗浄消毒後ATP値12,545(汚染物除去率56.5%)
【新規方法】
洗浄前ATP値26,708/洗浄消毒後ATP値97(汚染物除去率99.6%)
【考察】
■歯科用ミラーについて
従来の方法では45.5%もの汚れが残留していたのに対し、新規の方法では0.4%まで残留率が低下していた。これも洗浄の際、ミラー表面に付着していた汚れを、フィリオ30ナノが脂肪分やタンパクなどの粘性を低下させることで、より高率に剥離した事による効果だと考える。脂肪分やタンパク高分子などの分散効果により、殺菌剤の効きも当然高まっている
追加試験
【歯科用タービン(外側)における洗浄試験】
エタノールワッテによる拭取り
洗浄前ATP値1,625/洗浄消毒後ATP値363(汚染物除去率77.7%)
【歯科用ミラーにおける洗浄試験】
エタノールワッテによる拭取り
洗浄前ATP値27,591/洗浄消毒後ATP値12,545(汚染物除去率54.5%)
フィリオ30nanoクリーナー噴霧からティッシュペーパーによる拭取り
洗浄前ATP値26,708/洗浄消毒後ATP値97(汚染物除去率99.7%)
歯科におけるATP試験・2
【試験実施日】平成27年9月24日
【使用 除菌剤等】
・分散+弱酸性次亜塩素酸・洗浄除菌スプレー:フィリオ30nanoクリーナー
・次亜塩素酸弱酸性水: フィリオ30(5倍希釈)
【計測器具】
・ATP計測器:ルミテスター(キッコーマン製)
【洗浄対象物】
・シリコーン印象物(歯型)
・ミラー
・スポンジ
【その他】
・拭取用カットメン
【実験目的及び方法】
①シリコーン印象物(歯型)における洗浄試験
➡歯を印象物で歯型取り(下顎側全体)
➡型取り直後に印象物をATP測定(洗浄前)
わずかに濡らして顕微鏡観察用サンプルを採取
➡印象物を軽く水洗いし、ATP測定、及び、顕微鏡観察用サンプル採取
➡フィリオ30nanoクリーナーを噴霧して60秒放置後、ATP測定、及び、顕微鏡観察用サンプル採取
➡フィリオ30<5倍希釈>を噴霧後、ATP測定、及び、顕微鏡観察用サンプル採取
②ミラーにおける洗浄試験
➡使用後のミラーをATP測定(洗浄前)
➡フィリオ30nanoクリーナーをスプレーし、60秒放置後ATP試験
➡フィリオ30<5倍希釈>を噴霧し、カットメンで拭き取り後、ATP測定
③スポンジの洗浄試験 *手洗い
試験対象;新しいスポンジに水を吸わせ、シンクをこすったもの。
➡スポンジを絞り、絞り液をATP測定(洗浄前) 及び、顕微鏡用サンプル採取
➡フィリオ30nanoクリーナーでもみ洗いし、水道水で濯いだ後
絞り液をATP測定(洗浄後) 及び、顕微鏡用サンプル採取
④採取したサンプルの顕微鏡観察
【シリコーン印象物(歯型)における洗浄試験】
洗浄前ATP値225,771/水洗い後ATP値110,101(汚染物除去率48.8%)
フィリオ30nanoクリーナー洗浄後ATP値1,567(汚染物除去率99.3%)
フィリオ30(5倍希釈)ATP値916(タンパク除去率99.6%)
【ミラーにおける洗浄試験】
洗浄前ATP値151,498/フィリオ30nanoクリーナー洗浄後ATP値1,199(汚染物除去率99.2%)
フィリオ30(5倍希釈)ATP値223(汚染物除去率99.9%)
【スポンジの洗浄試験】
洗浄前ATP値648/フィリオ30nanoクリーナー洗浄後ATP値33(汚染物除去率95%)
歯科におけるATP試験・3
【試験実施日】
平成28年01月25日
【使用薬剤等】
・分散剤:ロータスクイーン(以降ロータス)
【計測器具】
・ATP計測器:ルミテスター PD-20(キッコーマン製)
【洗浄対象物】
・歯科用ミラー
・スポンジ
■試験状況
・歯科用ミラー(洗浄前)➡歯用スポンジで3人の口内を擦り、汚れを一つの容器に集めたものをミラーに付け、洗浄前の汚れとした。
【試験1】
洗浄前ATP値147,020/ロータスクィーン(原液)浸漬10秒し水洗い後ATP値609(汚染物除去率99.6%)
【試験2】
洗浄前ATP値218,255/ロータスクィーン(100倍希釈)浸漬5分し水洗い後ATP値521(汚染物除去率99.8%)
【試験3】
洗浄前ATP値145,619/ロータスクィーン(500倍希釈)超音波洗浄浸漬5分し水洗い後ATP値16(汚染物除去率99.99%)
【考察】
【歯科用ミラー】
試験1:ロータス原液および試験2:ロータス×100倍希釈では残留率は低いものの若干汚れが残留している状態でした。一方、試験3:×500倍希釈+超音波洗浄の結果は残留率が他の結果と比べ、1/20まで低下し高い洗浄力を発揮しました。



